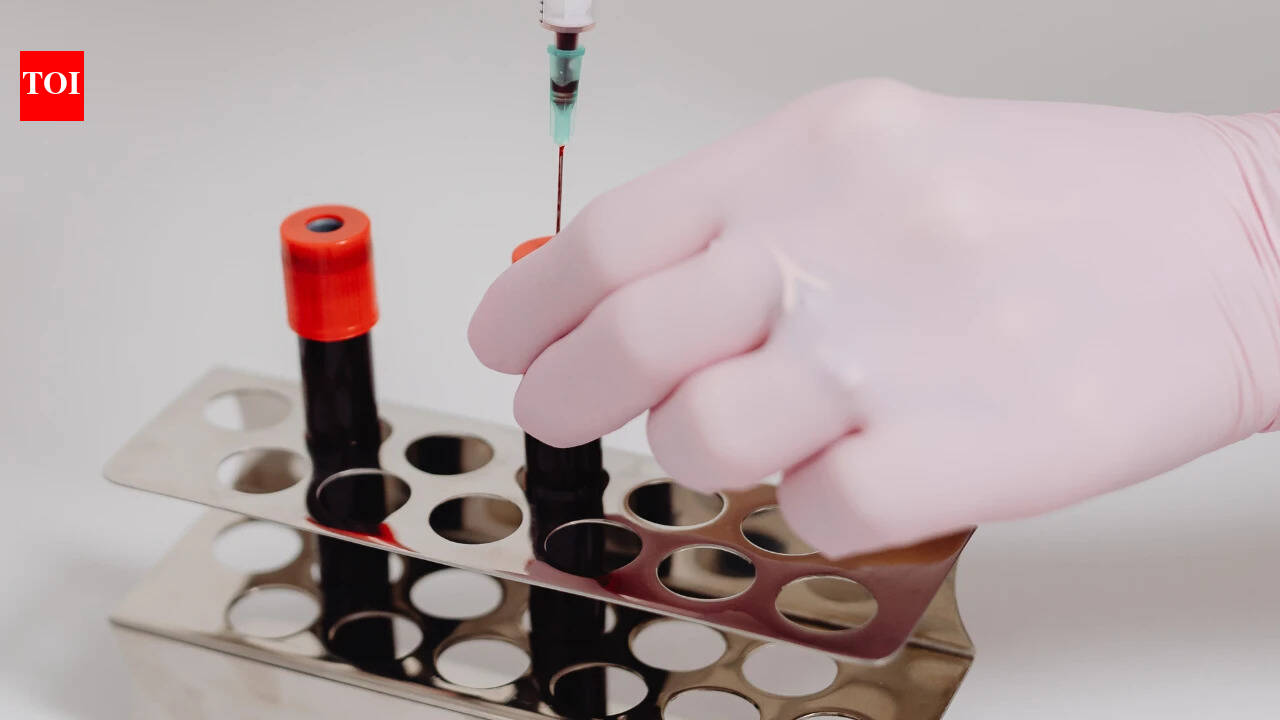
नई दिल्ली: केंद्र ने मानव प्लाज्मा से बनी दवाओं पर बार-बार वायरस परीक्षण रोकने के लिए दवा मानदंडों में संशोधन का प्रस्ताव दिया है, जिसमें कहा गया है कि इन उत्पादों का उत्पादन करने के लिए इस्तेमाल किए जाने वाले कच्चे प्लाज्मा का विनिर्माण शुरू होने से पहले ही एचआईवी और हेपेटाइटिस जैसे संक्रमणों के लिए परीक्षण किया जाता है।इन दवाओं में एल्ब्यूमिन, अंतःशिरा इम्युनोग्लोबुलिन (आईवीआईजी), और फैक्टर VIII और फैक्टर IX जैसे क्लॉटिंग कारक शामिल हैं, जिनका उपयोग प्रतिरक्षा विकारों, गंभीर संक्रमण और हीमोफिलिया जैसी रक्तस्राव स्थितियों के इलाज के लिए किया जाता है।अधिकारियों ने कहा कि इस कदम का उद्देश्य भारत के फार्मास्युटिकल नियमों को अंतरराष्ट्रीय फार्माकोपिया मानकों के अनुरूप बनाना है। वैश्विक दिशानिर्देशों की आवश्यकता है कि एकत्रित प्लाज्मा को अंशांकन के लिए उपयोग करने से पहले हेपेटाइटिस बी सतह एंटीजन, हेपेटाइटिस सी वायरस आरएनए और एचआईवी एंटीबॉडी के लिए परीक्षण किया जाए, और केवल प्लाज्मा जो नकारात्मक परीक्षण करता है वह प्लाज्मा-व्युत्पन्न दवाओं के निर्माण के लिए अधिकृत है।वर्तमान में, इन दवाओं को बनाने के लिए एकत्र किए गए प्लाज्मा को पहले एकत्र किया जाता है और एचआईवी, हेपेटाइटिस बी और हेपेटाइटिस सी सहित वायरस के लिए परीक्षण किया जाता है। हालांकि, एक बार जब इस परीक्षण किए गए प्लाज्मा से दवाओं का उत्पादन किया जाता है, तो तैयार उत्पादों को मौजूदा नियमों के अनुसार उसी वायरल मार्करों के लिए फिर से परीक्षण किया जाता है। सरकार अब परीक्षण के इस दूसरे दौर को खत्म करने का प्रस्ताव रखती है।स्वास्थ्य मंत्रालय ने एक मसौदा अधिसूचना जारी की है जिसमें औषधि नियम, 1945 में संशोधन पर सार्वजनिक टिप्पणियां मांगी गई हैं, जो रक्त उत्पादों के परीक्षण को विनियमित करते हैं। मेदांता, गुरुग्राम के ट्रांसफ्यूजन मेडिसिन विभाग के वरिष्ठ निदेशक डॉ. असीम कुमार तिवारी ने कहा कि प्लाज्मा फ्रैक्शनेटर विभिन्न जीवन रक्षक दवाओं के निर्माण के लिए रक्त दाताओं से एकत्र किए गए अधिशेष प्लाज्मा का उपयोग कर सकते हैं।उन्होंने कहा, “प्लाज्मा-व्युत्पन्न दवाएं (पीडीएमपी), जैसे एल्ब्यूमिन, अंतःशिरा इम्युनोग्लोबुलिन (आईवीआईजी), और क्लॉटिंग कारक जैसे फैक्टर VIII और फैक्टर IX, का व्यापक रूप से प्रतिरक्षा विकारों, गंभीर संक्रमण और हीमोफिलिया जैसी रक्तस्राव स्थितियों के इलाज के लिए उपयोग किया जाता है।”उन्होंने कहा कि रक्त केंद्र अक्सर मरीजों की जरूरतों को पूरा करने के बाद अधिशेष प्लाज्मा उत्पन्न करते हैं, जिसे विशेष अंशीकरण सुविधाओं में आपूर्ति की जा सकती है जहां इन दवाओं के निर्माण के लिए विभिन्न प्रोटीनों को अलग किया जाता है।डॉ. तिवारी ने कहा कि मरीजों तक पहुंचने से पहले पीडीएमपी को कई सुरक्षा जांचों से गुजरना पड़ता है। उन्होंने कहा, “दान किए गए प्लाज्मा का एचआईवी, हेपेटाइटिस बी, हेपेटाइटिस सी, मलेरिया और सिफलिस जैसे संक्रमणों के लिए परीक्षण किया जाता है और निर्माण प्रक्रिया में सुरक्षा सुनिश्चित करने के लिए वायरल निष्क्रियता चरण शामिल होते हैं।”उन्होंने कहा, “दुनिया भर में प्लाज्मा-व्युत्पन्न औषधीय उत्पादों के रूप में जानी जाने वाली इन दवाओं को विनिर्माण के दौरान कठोर परीक्षण और वायरल निष्क्रियता के कारण संक्रमण के संचरण से नहीं जोड़ा गया है।”अधिकारियों का कहना है कि तैयार उत्पाद चरण में समान वायरल परीक्षणों को दोहराने से दोहराव पैदा होता है जो वैश्विक प्रथाओं के तहत आवश्यक नहीं है। प्रस्तावित संशोधन का उद्देश्य प्लाज्मा पहचान चरण में सख्त सुरक्षा नियंत्रण बनाए रखते हुए परीक्षण आवश्यकताओं को सुव्यवस्थित करना है।ड्रग तकनीकी सलाहकार बोर्ड के परामर्श के बाद मसौदा नियम जारी किए गए थे, और संशोधन को अंतिम रूप देने से पहले इच्छुक पार्टियों को टिप्पणियां प्रस्तुत करने के लिए 30 दिन का समय दिया गया था।
सरकार ने प्लाज्मा-आधारित दवाओं पर बार-बार होने वाले वायरस परीक्षण को खत्म करने का प्रस्ताव रखा है | भारत समाचार